Los resultados de la investigación sobre "Eficacia y seguridad de dos pautasde suplementos vitamínicos sobre los nivelesde homocisteína en pacientes en hemodiálisis. Ensayo clínico prospectivo y randomizado" llevadas a cabo por J. E. Sánchez Álvarez, L. Pérez Tamajón, D. Hernández, A. Álvarez González, P. Delgado, V. Lorenzo (Sánchez Álvarez JE, Pérez Tamajón L, Hernández D, Álvarez González A, Delgado P, Lorenzo V. Eficacia y seguridad de dos pautas de suplementos vitamínicos sobre los niveles de homocisteína en pacientes en hemodiálisis. Ensayo clínico prospectivo y randomizado. Nefrologia 2005;25:288-96.).
La hiperhomocisteinemia (HHcys) es frecuente en pacientes urémicos y representa un factor de riesgo cardiovascular. Los suplementos vitamínicos reducen los niveles de homocisteína (Hcys), no estando bien definida la dosis óptima y su eficacia. El genotipo de la metilentetrahidrofolatoreductasa (MTHFR) puede modular su prevalencia y respuesta al tratamiento.
Objetivo: Conocer la eficacia de dos pautas de suplementos vitamínicos sobre los niveles de Hcys tras 12 meses de tratamiento.
Metodología: Estudio prospectivo, randomizado, a doble ciego. Sesenta pacientes en hemodiálisis se aleatorizaron en dos grupos terapéuticos: A) Dosis habituales de ácido fólico (AcF), vitamina B6 y B12 a la dosis de 5, 10 y 0,4 mg diarios, respectivamente (N = 27) y B) Dosis suprafisiológicas (15, 100 y 1 mg diarios) (N = 33). Los valores de Hcys se compararon con un grupo control similar en edad y sexo.
Resultados: Todos los pacientes y el 22% de los controles presentaron HHcys siendo los niveles de Hcys 2,5 veces superiores en los pacientes que en el grupo control (32,4 ± 8,9 vs 12,9 ± 6,8 µmol/L; P < 0,0001). Las dos pautas fueron igualmente eficaces en reducir la Hcys, aunque solamente el 12% de los pacientes normalizaron sus niveles al finalizar el estudio. Globalmente, los niveles de Hcys experimentaron un descenso significativo al mes de tratamiento (23,6%, P < 0,001). El mayor descenso se registró tras 6 meses (28,3%, P < 0,001), estabilizándose hasta los 12 meses. El mayor descenso de Hcys se asoció con niveles basales más altos de Hcys (r = 0,500, P < 0,001) y más bajos de AcF (r = -0,332, P = 0,009). El polimorfismo de la MTHFR no modificó significativamente la respuesta terapéutica.
Conclusiones: La HHcys es constante con pautas convencionales de hemodiálisis aunque no existan déficits vitamínicos. Los suplementos reducen de forma substancial y sostenida los niveles de Hcys. Dosis suprafisiológicas no suponen ventajas adicionales. Se requieren nuevos estudios para demostrar que este descenso conlleve un impacto final favorable sobre la morbi-mortalidad cardiovascular.
INTRODUCCIÓN
La existencia de una población cada vez más envejecida, ateromatosa y diabética en diálisis justifica el creciente interés y preocupación que han despertado los problemas cardiovasculares (CV) en ella. Las complicaciones CV representan entre el 45-50%[1] de todas las causas de muerte en diálisis y la mortalidad de causa CV es claramente superior en la uremia que en la población general[2]. De hecho, en los enfermos con insuficiencia renal, a los clásicos factores de riesgo de morbilidad cardiovascular descritos en la población general[3][4], se le añaden aquellos relacionados con el propio estado urémico como son el hiperparatiroidismo secundario, la anemia, y la uremia per se[5].
La hiperhomocisteinemia (HHcys) es un factor de riesgo de arteriosclerosis y enfermedad vaso-oclusiva, en la población general[6] y en la insuficiencia renal[7]. La HHcys es un fenómeno universal en la población urémica, siendo los niveles de homocisteína (Hcys) 2-3 veces superiores a sus equivalentes en edad y sexo de la población general[8]. Su origen es multifactorial e incluye la predisposición genética[9], el déficit nutricional de cofactores del metabolismo de la Hcys[10][11][12] y la propia insuficiencia renal[13]. Parece ser que el propio estado urémico es el que condiciona el aumento en los niveles de Hcys. De ser así, cabría esperar que una mayor dosis de diálisis tenga un impacto favorable sobre los niveles de Hcys, tal como un reciente trabajo[14] parece confirmar.
Se ha demostrado que los suplementos de vitamina B6, B12 y ácido fólico (AcF) reducen eficazmente los niveles de Hcys en la población general[15][16]. Sin embargo, en la población urémica, el tratamiento con vitaminas ha alcanzado resultados más modestos[17][18][19][20]. Estos estudios han sido efectuados en períodos de seguimiento relativamente cortos, con escaso número de pacientes y la dosis óptima no ha sido establecida. Además existe controversia sobre si el descenso en los niveles de Hcys supone un beneficio[21] o no[22] sobre la supervivencia del enfermo.
Nosotros planteamos un ensayo clínico prospectivo y randomizado para conocer el efecto de dos pautas de suplementos vitamínicos sobre los niveles de Hcys tras 12 meses de tratamiento en una población estable en hemodiálisis. Además, estudiamos la prevalencia de HHcys y su relación con los niveles séricos de vitaminas B6, B12 y AcF. Adicionalmente evaluamos la influencia del polimorfismo de la enzima metilentetrahidrofolatoreductasa (MTHFR) sobre los niveles de Hcys y la respuesta al tratamiento.
MATERIAL Y MÉTODOS
Pacientes
Todos los pacientes en programa de hemodiálisis (HD) en el Hospital Tamaragua (Puerto de la Cruz, Tenerife) a fecha abril/2002 fueron evaluados para el presente estudio. La pauta de diálisis era de 1213,5 hs semana, en modalidad trisemanal, con un porcentaje de reducción de urea prescrito 65%, empleando un dializador de polisulfona F8 (Fresenius. Bad Homburg. Germany).
Se consideraron criterios de inclusión:
- Pacientes de ambos sexos, mayores de 18 años, clínicamente estables, definido como ausencia de complicaciones que hayan requerido ingreso en los últimos 3 meses, a excepción de las relacionadas con disfunción del acceso vascular.
- Llevar más de 6 meses en programa de HD.
- Test de embarazo negativo en las mujeres.
- Ausencia de reacción conocida o eventual intolerancia al complejo vitamínico.
Como criterios de exclusión se consideraron:
- Recibir fármacos que pudieran influir sobre los niveles séricos de Hcys, o su metabolismo en los 30 días previos al inicio del estudio.
- Reconocida mala adherencia al tratamiento y a las indicaciones médicas.
Diseño del ensayo
Se diseñó un ensayo clínico prospectivo, randomizado, controlado, a doble ciego con grupos paralelos, para estudiar un complejo vitamínico autorizado, a dos dosis diferentes, durante un período de tratamiento de 12 meses.
De los 87 pacientes inicialmente evaluados, 60 cumplieron los criterios de inclusión y exclusión. Un mes antes de iniciar el tratamiento los pacientes suspendieron la ingesta de complejos vitamínicos que tuvieran AcF, vitamina B6 y B12.
Los pacientes fueron randomizados en dos grupos terapéuticos: Grupo A (dosis habituales) complejo vitamínico compuesto por AcF 5 mg, Vitamina B6 10 mg, Vitamina B12 0,4 mg), y Grupo B (dosis suprafisiológicas) el mismo complejo a las dosis de AcF 15 mg, Vitamina B6 100 mg, Vitamina B12 1 mg). El tratamiento consistía en la toma de una cápsula diaria y la presentación del compuesto era idéntica en ambos grupos. Se emplearon dosis fijas durante todo el período de tratamiento. Todos los pacientes continuaron con su medicación habitual.
El ensayo clínico fue aprobado por el Comité Ético del Hospital Universitario de Canarias y del Hospital Tamaragua. Todos los pacientes dieron su consentimiento informado por escrito para participar en el estudio.
Etapas de desarrollo (cronograma)
Antes del inicio se realizó una anamnesis y examen físico. Además de la analítica general, se extrajo una muestra para determinación genética. Mensualmente fueron registradas las posibles incidencias y efectos adversos que pudieran estar relacionados con la medicación a estudio y se realizaba una analítica general. Al 1°, 3°, 6° y 12° mes se determinaron los niveles séricos de Hcys, AcF y vitaminas B6 y B12.
Aquellos pacientes que no completaron el estudio por trasplante renal o exitus, fueron excluidos del estudio longitudinal, pero se analizaron los resultados basales según la intención de tratar.
Estimación del tamaño muestral y codificación
Para la estimación del tamaño de la muestra se utilizó un trabajo previo de Bostom y cols[17]. Estos autores empleando dosis suprafisiológicas de un complejo vitamínico similar al nuestro, observaron que los niveles de Hcys descendieron significativamente respecto al grupo control (-26,2% vs +1,6%, p = 0,027). En base a estos resultados, nosotros estimamos que para detectar una diferencia en el descenso de Hcys del 25% entre los dos grupos, con un poder estadístico del 80% (Beta = 0,2), más un riesgo estadístico de primera especie del 5% (alfa = 0,05) y unas pérdidas previstas durante el seguimiento del 10%, se requerían 60 pacientes (30 en cada grupo) para una evaluación de la eficacia del tratamiento (StatXact5®, Cytel Software Corporation, Massachusetts).
El código de randomización (tabla de números aleatorios, StatXact5) fue preparado por el Servicio de Farmacia del Hospital Universitario de Canarias (La Laguna, Tenerife) y se entregó mediante cápsulas al investigador principal en el momento de la inclusión de los pacientes. Se comprobó el cumplimiento terapéutico mediante el retorno de los envases por parte del paciente y el recuento de los mismos por parte del investigador.
Grupo control
Se obtuvo un grupo de 276 voluntarios sanos, a fin de conocer los valores de referencia de Hcys, AcF y Vitamina B12 (en el grupo control no se determinaron niveles de vitamina B6).
Determinaciones bioquímicas
Tabla I. Parámetros demográficos y valores bioquímicos basales de ambos grupos terapéuticos. Tanto las características demográficas como los niveles séricos de Hcys y de las tres vitaminas fueron similares entre grupos
| Total | Grupo 1 | Grupo 2 | |
|---|---|---|---|
| N | 60 | 30 | 30 |
| Edad (años) | 68 ± 13 | 64 ± 14 | 70 ± 10 |
| % Varones | 48 | 48 | 48 |
| % Diabéticos | 50 | 50 | 50 |
| % HTA | 13 | 14 | 12 |
| Hcys (μmol/L) | 32,4 ± 8,9 | 32,7 ± 7,9 | 32,1 ± 9,8 |
| AcF (nmol/L) | 7,74 ± 7,3 | 8,0 ± 9,6 | 7,5 ± 4,8 |
| B12 (pmol/L) | 546,6 ± 222 | 516,8 ± 185 | 570,9 ± 248 |
| B6 (nmol/L) | 32,9 ± 49,4 | 31,1 ± 47,7 | 34,4 ± 51,5 |
Las muestras sanguíneas fueron extraídas al inicio de la sesión de HD de la mitad de la semana. La analítica general se realizó por autoanalizador, empleando técnicas rutinarias. Los niveles de AcF y Vitamina B12 se determinaron simultáneamente por método radiométrico (SPNB, Dualcount Folic Acid/ Vitamin B12 in vitro Diagnostic Test Kit; Diagnostic Products Corporation; Los Ángeles, California); los valores normales de referencia del ensayo para el AcF eran entre 3,0-17,0 nmol/L y para la Vitamina B12 de 200-950 pmol/L). La Vitamina B6 se determinó por método radioenzimático (valores de referencia 20-160 nmol/L).
Los niveles de homocisteína total (la suma de la forma libre y la unida a proteínas) se determinaron utilizando un inmunoensayo de polarización fluorescente (IMX, Abbot Diagnostics, Abbot Park, IL).
Genotipo de la MTHFR
El ADN del paciente se sometió a dos amplificaciones alelo-específicas mediante reacción en cadena de polimerasa (PCR), utilizando un oligonucleótido común y otro específico, bien para el alelo Ala223 o para el alelo Val223. El diseño de los «primers» se hizo a partir de la secuencia depositada en GenBank (U09806).
Análisis estadístico
Las variables continuas se expresaron como media y desviación típica y las categóricas como porcentaje. Los valores basales de ambos grupos terapéuticos se compararon mediante T test y Chi Cuadrado según procediese. Previamente se había empleado el test de KoImogorov-Smirnov para ver si seguían una distribución normal. Para analizar los niveles de Hcys durante el periodo de estudio se utilizó el modelo lineal general con medidas repetidas. Los cambios porcentuales de Hcys, y los absolutos entre los dos grupos de tratamiento se compararon mediante t Test o la U de Mann-Whitney según procediera. Para las correlaciones univariadas se empleo la r de Pearson.
Para conocer los mejores predictores de Hcys basal y de respuesta al tratamiento se aplicó un modelo de regresión lineal. Se utilizó el paquete estadístico SPSS 11.1® para Windows (SPSS Inc, Chicago, IL) para el análisis de los resultados.
RESULTADOS
Parámetros basales
Se incluyeron finalmente 60 pacientes. En la tabla I se muestran los datos demográficos y bioquímicos basales de todos los pacientes y de ambos grupos terapéuticos.
En la figura 1 se comparan los valores basales de Hcys, AcF y vitamina B12 entre el grupo total de pacientes y el grupo control. Los valores medios basales de Hcys resultaron 2,5 veces más elevados en los pacientes que en los controles.
Definimos HHcys cuando sus niveles séricos eran superiores a 15 µmol/L[23]. Aplicando este corte, en la figura 1A podemos ver que el 100% de los pacientes y el 22% de los controles tenía HHcys, respectivamente. Las figuras 1B y 1C demuestran que los niveles basales de AcF y B12 respectivamentes fueron significativamente más elevadas en los pacientes que en el grupo control.
Predictores de los niveles basales de Hcys
En el análisis univariado, los niveles de Hcys basal sólo se correlacionaron inversamente con los niveles basales de AcF (r = -0,340, P = 0,008). No hallamos asociación de los niveles basales de Hcys con otros parámetros bioquímicos (niveles de vitamina B6, B12, perfil lipídico, glucosa, BUN, albumina) ni demográficos (edad, sexo, tiempo en HD, diabetes o HTA).
Para conocer los mejores predictores de los niveles basales de Hcys empleamos un modelo de regresión lineal incluyendo parámetros demográficos, bioquímicos y el genotipo de la MTHFR como variables independientes. Bajo este modelo, solamente los niveles basales de AcF resultaron predictores independientes de la Hcys (B = -0,75 [IC95% = -1,21, -0,30], P < 0,001).
Respuesta al tratamiento
De los 60 pacientes iniciales, 54 completaron el estudio, tres se trasplantaron y tres fallecieron. El tratamiento fue bien tolerado, no apareciendo ningún efecto secundario ni abandono de la medicación por este motivo. En la figura 2 se representa la progresión de los niveles de AcF, B12 y B6 durante el periodo de tratamiento en los dos grupos terapéuticos. Estos datos confirmaron la adecuada adherencia al tratamiento de los pacientes observada en la supervisión de la recogida de los envases de la medicación. Los niveles de AcF y de vitaminas subieron de forma significativa en cada grupo, especialmente durante el primer trimestre. A pesar de recibir dosis diferentes, las diferencias de niveles entre ambos grupos no fueron relevantes, excepto para el AcF en el 6° mes de tratamiento (14,74 ± 8,20 vs 26,48 ± 28,22 nmol/L, p < 0,003).

Figura 1.
–En las figuras 1A, 1B y 1C se comparan los valores (X ± DS) de Hcys, AcF y B12 respectivamente, entre los pacientes y el grupo control. En la figura lA la línea de puntos representa el valor de 15 µmol/L tomado como umbral de referencia.

Figura 2.
–Niveles de AcF, B12 y B6 durante el periodo de tratamiento en los dos grupos terapéuticos (SF: dosis suprafisiológicas; H: dosis habituales).
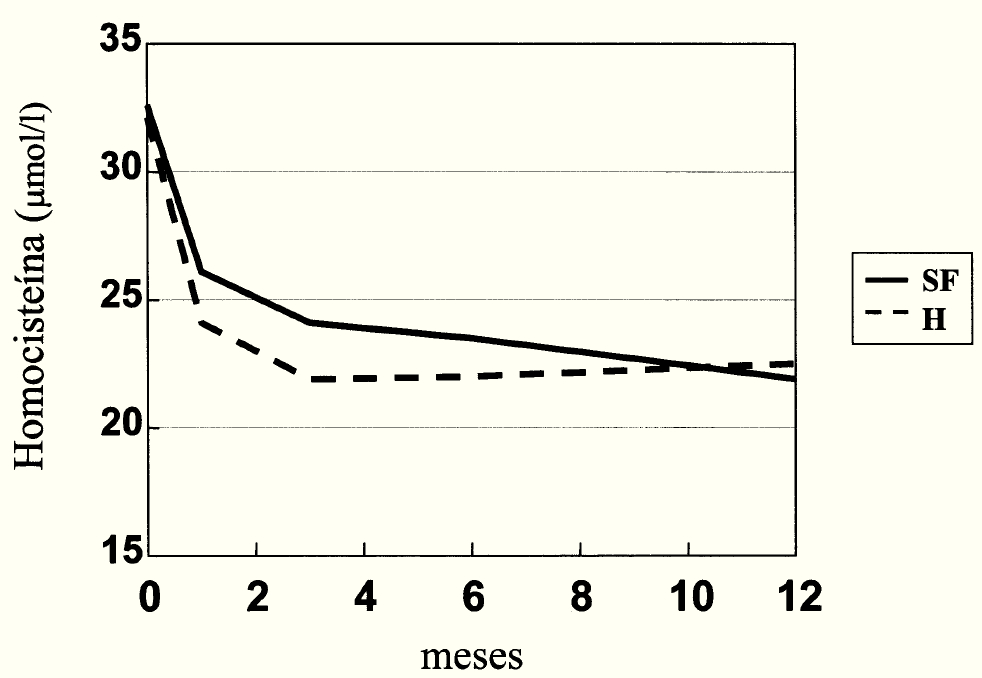
Figura 3.
–Niveles de Hcys durante el período de tratamiento en los dos grupos terapéuticos (SF: dosis suprafisiológicas; H: dosis habituales).
Globalmente los niveles de Hcys descendieron un 24% durante el primer mes. El mayor descenso se observó al 6° mes (28,3%), para mantenerse prácticamente estables durante todo el período de seguimiento. En la figura 3 se representa el efecto de ambas pautas de tratamiento sobre los niveles de Hcys. Con el empleo de las dosis habituales, los niveles de Hcys descendieron un 20, 26, 30 y 33% al 1°, 3°, 6° y 12° mes de tratamiento respectivamente. Un descenso similar de 22, 28, 27 y 24% se observó en los pacientes que recibieron dosis suprafisiológicas.
A pesar de que el empleo del suplemento vitamínico fue eficaz para descender los niveles de Hcys, este fue subóptimo, ya que solo el 12% de los pacientes normalizaron los valores Hcys. En la figura 4 se representan las variaciones en los niveles de Hcys antes y a los 12 meses del tratamiento.
Predictores de la respuesta al tratamiento
En el análisis univariado observamos que el delta ( ) de descenso de Hcys (porcentaje de descenso respecto al basal) tras 12 meses de tratamiento se asoció de forma directa con los niveles basales de Hcys (r = 0,500, P < 0,001) e inversa con los niveles basales de AcF (r = -0,332, P = 0,009) (figs. 5A y 5B). Otros parámetros demográficos (edad, sexo, diabetes, tiempo en HD) y bioquímicos (niveles basales de B6 y B12, perfil lipídico, glucemia, albumina o BUN) no tuvieron efecto. En el modelo de regresión lineal multivariado solamente los niveles basales de Hcys (B = 0,97 [IC95% = 0,39, 1,54], P < 0,001) fueron predictores de la respuesta al tratamiento.
Efecto del Polimorfismo del gen de la MTHFR
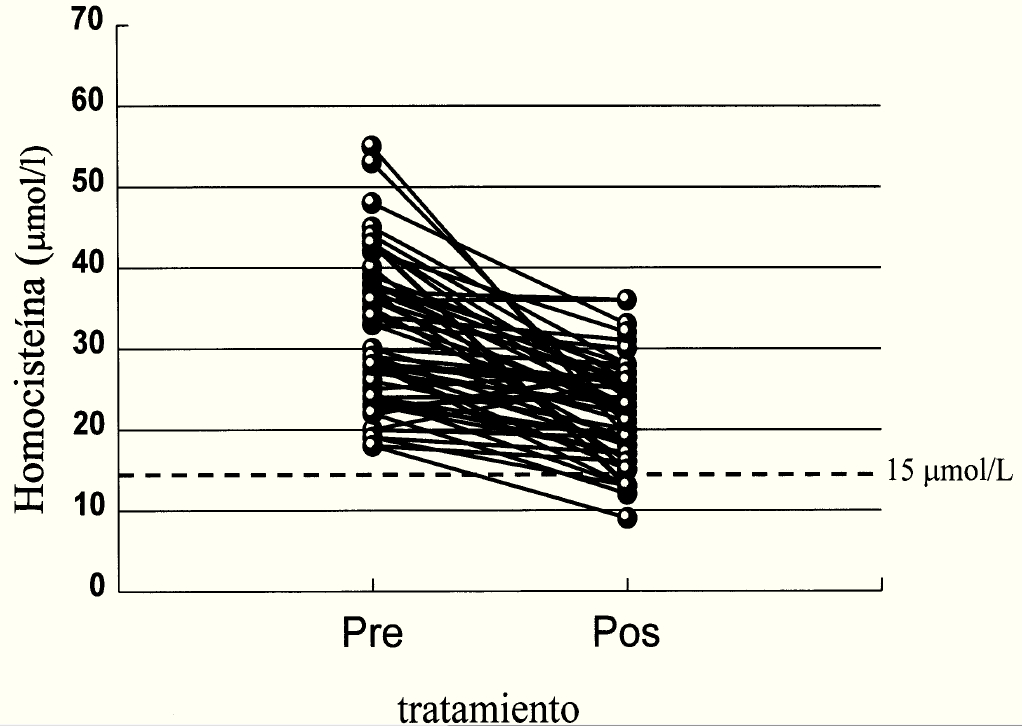
Figura 4.
–Valores individuales de Hcys basales y a los 12 meses de tratamiento. La línea de puntos representa el valor de Hcys de 15 µmol/L.
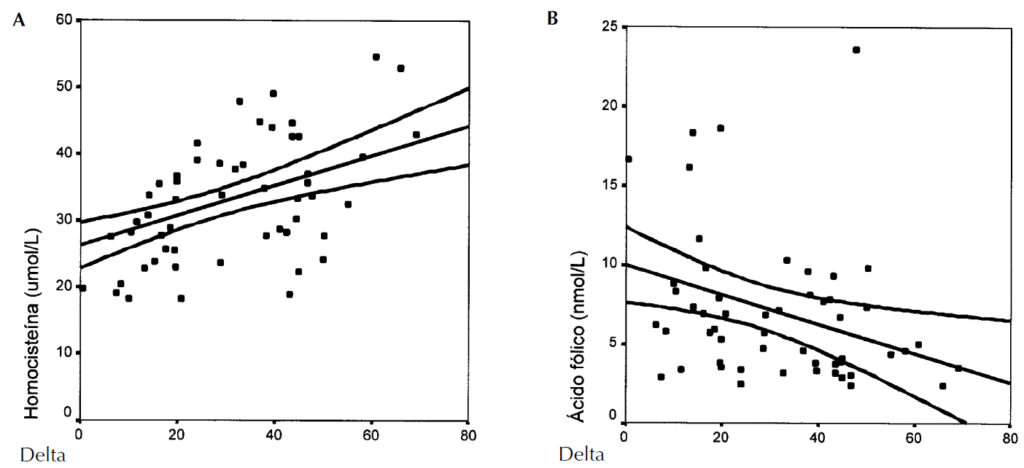
Figura 5.
–Correlación entre el delta del descenso de homocisteína y los niveles basales de homocisteína (fig. 5A) y los de ácido fólico (fig. 5B).
Nuestros pacientes se agruparon de la siguiente forma en relación al polimorfismo del gen de la MTHFR: 7 de ellos (12%) eran portadores del genotipo desfavorable (VV); del resto, 24 pacientes (40%) portaban el genotipo A-A y 29 (48%) el AV. Estas proporciones son similares a las descritas en la población general[17][21].
En relación a su influencia, pudimos observar que no hay diferencias significativas entre los niveles de Hcys, AcF, ni los delta de Hcys entre aquellos pacientes con genotipo desfavorable y los poseedores del genotipo favorable.
DISCUSIÓN
Este trabajo revela que la HHcys es prácticamente universal en los pacientes en HD a pesar de no tener déficit vitamínico. Los resultados del ensayo clínico demuestran que un complejo de vitaminas hidrosolubles (AcF, vitamina B6 y B12), económico y seguro, en dos dosis diferentes es eficaz para reducir los niveles de Hcys, aunque solamente en un pequeño porcentaje alcanza el rango de normalidad.
Los criterios usados para definir HHcys no son uniformes en la literatura[6][17][18][24]
[25]. Esto es debido a las características y diseño de cada estudio. Algunos autores la han definido en base al valor por encima del cual se incrementa significativamente el número de eventos CV o de lesiones ateroscleróticas o arterioscleróticas del árbol vascular[26]. Otros, han aplicado los rangos extremos de su serie, en términos de percentiles o desviaciones típicas[27][28]. A pesar de estas discrepancias, valores entre 12 y 16 µmol/L son empleados por la mayoría de los autores como valor de corte por encima del cual se define HHcys. Aplicando 15 µmol/L como punto de corte[23], coincidimos con otros autores, en que prácticamente el 100% de los pacientes en HD presenta HHcys.
Los niveles séricos de vitaminas son muy variables, tanto en la población general[24][29][30] como en la población urémica7, 31, 32. En pacientes en diálisis se han descrito valores altos18, normales31 o bajos19. Es notable que varios autores han destacado que la HHcys ocurre en los pacientes en HD a pesar de presentar niveles normales y hasta supranormales de vitaminas[7][17][33]. De hecho, en nuestra población control los niveles de vitaminas fueron más bajos que en los enfermos, aunque la media y mediana de estos valores cayeron dentro del rango de normalidad en ambas poblaciones. Estos datos sugieren que no es el déficit vitamínico ni las pérdidas por el dializado lo que condiciona la HHcys del enfermo en diálisis y que otros factores relacionados con la propia uremia deben estar implicados.
Bostom y cols[17] demostraron el efecto beneficioso de dosis suprafisiológicas de vitaminas (16 mg/día de AcF) respecto a un grupo control (AcF 1 mg/día) alcanzando un descenso de los niveles de Hcys del 30% versus un 2% respectivamente, tras ocho semanas de tratamiento. Nosotros empleamos dos dosis deferentes del complejo vitamínico, logrando un efecto similar en ambos casos y idéntico al conseguido por Bostom con las dosis suprafisiológicas de su complejo. Otros autores empleando una combinación de complejos vitamínicos y diferentes pautas[17][25][32][33][34] han descrito resultados similares, es decir, los niveles de Hcys descienden en torno al 20-35%, pero solo una pequeña proporción alcanza valores normales. Los tiempos de tratamiento en estas series, en general, no han superado los 6 meses. Tremblay y cols[18] estudiaron el efecto de estos suplementos vitamínicos en 168 pacientes en HD durante 12 meses. Todos ellos recibieron diariamente un complejo multivitamínico (1 mg AcF, 10 mg B6, 6 µg B12). Y además a la mitad se les administraron 10 mg iv de AcF postdiálisis. Observaron un descenso medio de los niveles de Hcys del 23,5% a los 6 meses y del 21,7 al año. El grupo con dosis extra de AcF postdiálisis experimentó un descenso significativamente mayor que el otro grupo a los 6 meses, pero no se observó esa diferencia al año.
Nuestro estudio se diseñó también a largo plazo, 12 meses, observando que una vez alcanzado un nivel máximo de descenso –al sexto mes–, los niveles de Hcys se mantienen estables. Es destacable la estabilización en el descenso de Hcys, sin llegar a normalizarse. Diversos factores se han propuesto para explicar esta circunstancia que van desde la pérdida de metabolización renal[13] hasta la caída del filtrado glomerular[35]. Esto explicaría el aumento de Hcys en la insuficiencia renal pero no el agotamiento del efecto de las vitaminas.
Otras observaciones a tener en cuenta en este estudio son:
- que existe una relación inversa entre los niveles basales de Hcys y AcF, pero no con los de vitamina B;
- que niveles basales más bajos de AcF y más altos de Hcys son predictores independientes de la eficacia del tratamiento, y
- que niveles elevados de Hcys estuvieron presentes aun en aquellos pacientes correspondientes al cuartil alto de folemia (AcF > 8,7 nmol/L).
Todo esto sugiere que el efecto del AcF sobre los niveles de Hcys es cuantitativamente más relevante que el de la Vit B, y que factores relacionados con propio estado urémico condicionan una resistencia al efecto de las vitaminas.
El presente ensayo demuestra que el complejo vitamínico a las dosis empleadas reduce eficazmente y de forma sostenida los niveles Hcys. Sin embargo solamente en el 12% de los enfermos se normalizaron los niveles de Hcys. Estos resultados aunque aparentemente subóptimos, no deberían considerarse ineficaces. Se ha observado que la mortalidad se asocia a un incremento proporcional de los niveles de Hcys en pacientes con enfermedad coronaria36. Un amplio meta-análisis de estudios efectuados en la población general ha demostrado que por cada 3 µmol/L de descenso de Hcys, se reduce el riesgo de enfermedad isquémica coronaria, trombosis venosa profunda y accidente cerebrovascular en un 16, 25 y 24% respectivamente[37]. Asumiendo que ocurra lo mismo en los pacientes en HD, cualquier descenso que se consiga en los niveles de Hcys debería tener un impacto favorable sobre la morbi-mortalidad CV en esta población. Por ello, considerando la alarmante magnitud de las complicaciones CV en HD, parece razonable proponer el empleo rutinario de estos suplementos vitamínicos inocuos y económicos, a dosis estándar, en estos enfermos. Dado el carácter universal de la HHcys en HD el empleo de estas vitaminas, aun cuando no se disponga de determinaciones séricas rutinarias de Hcys, es un aspecto a considerar.
Respecto a la influencia del gen de la MTHFR nuestros resultados están claramente limitados por el tamaño de la muestra (el genotipo desfavorable está representado solamente en 7 pacientes). Es bien conocido que se requieren muestras amplias para identificar asociaciones entre polimorfismos y observaciones clínicas o resultados terapéuticos. Con los datos observados por nosotros, no podemos decir que el polimorfismo de la MTHFR tenga una influencia sobre los niveles basales de Hcys ni sobre la respuesta al tratamiento.
En conclusión, la HHcys es constante en pacientes con pautas convencionales de HD a pesar de no presentar déficit vitamínicos. Sin embargo, el presente ensayo clínico demuestra un efecto beneficioso, aunque subóptimo, de los suplementos vitamínicos a dos dosis diferentes sobre los niveles de Hcys. De estas observaciones cabe deducir que el propio estado urémico condiciona una resistencia parcial al efecto de las vitaminas. Y de ser así, cabría esperar que una mayor dosis de diálisis tenga un impacto favorable sobre los niveles de Hcys. Si el efecto beneficioso de estas modalidades terapéuticas sobre los niveles de Hcys, conlleva un impacto final favorable sobre la morbilidad y mortalidad cardiovascular, es un aspecto fundamental que aun debe ser demostrado.
BIBLIOGRAFÍA
- U.S. Renal Data System; USRDT 2002. Annual Data Report: National Institute of Heath, National Institute of Diabetes and Digestive and Kidney Diseases, Bethesda, MD, 2002.
- Foley RN, Parfrey PS, Sarnak MJ: Clinical epidemiology of cardiovascular disease in chronic renal disease. Am J Kidney Dis 32: 5112-5119, 1998.
- Ma K, Greene E, Raij L: Cardiovascular risk factors in chronic renal failure and hemodialysis populations. Am J Kidney Dis 21: 505-513, 1992.
- Rostand S, Brunzell J, Cannon R, Victor R: Cardiovascular complications in renal failure. J Am Soc Nephrol 2: 10531062, 1991.
- Ayus JC, Lorenzo V, Hernández D: Complicaciones cardíacas en la insuficiencia renal crónica y después del trasplante renal. En: Llach F, Valderrábano F (eds.): Insuficiencia Renal Crónica. Diálisis y Trasplante Renal. Ediciones Norma, Madrid. pp. 173-198, 1997.
- Boushey CJ, Beresford SA, Omenn GS, Motulsky AG: A quantitative assessment of plasma homocysteine as a risk factor for vascular disease: probable benefits of increasing folic acid intakes. JAMA 274: 1049-1057, 1995.
- Manns B, Burgess E, Hyndman ME, Parsons HG, Schaefer JP, Scott-Douglas NW: Hyperhomocysteinemia and the prevalence of atherosclerotic vascular disease in patients with endstage renal disease. Am J Kidney Dis 34: 669-677, 1999.
- Bostom A, Lathrop L: Hyperhomocysteinemia in end-stage renal disease: prevalence, etiology, and potencial relationship to arteriosclerotic outcomes. Kidney Int 52: 10-20, 1997.
- Fodinger M, Mannhalter C, Wolfl G, Pabinger I, Muller E, Schmid R, Horl WH, Sunder-Plassmann G: Mutation (677 C to T) in the methylenetetrahydrofolate reductase gene aggravates hyperhomocysteinemia in hemodialysis patients. Kidney Int 52(2): 517-523, 1997.
- Bachmann J, Tepel M, Raidt H, Riezler R, Graefe U, Langer K y cols.: Hyperhomocysteinemia and the risk for vascular disease in hemodialysis patients. J Am Soc Nephrol 6(1): 121125, 1995.
- Bostom AG, Shemin D, Lapane KL, Nadeau MR, Sutherland P, Chan J, Rozen R, Yoburn D, Jacques PF, Selhub J, Rosenberg IH: Folate status is the major determinant of fasting total plasma homocysteine levels in maintenance dialysis patients. Atherosclerosis 123: 193-202, 1996.
- Van Guldener C, Janssen MJ, De Meer K, Donker AJ, Stehouwer CD: Effect of folic acid and betaine on fasting and postmethionine-loading plasma homocysteine and methionine levels in chronic haemodialysis patients. J Intern Med 245(2): 175-83, 1999.
- Van Guldener C, Stam F, Stehouwer CDA: Homocysteine metabolism in renal failure. Kid Intern 59 (Supl. 78): 234-237, 2001.
- Maduell F, Navarro V, Torregrosa E, Ríus A, Dicenta F, Cruz MC, Ferrero JA: Change from three times a week on-line hemodiafiltration to short daily on-line hemodiafiltration. Kidney Int 64: 305-13, 2003.
- Ubbink J, Hayward Vermaak WJ, Merwe A, Becker PJ, Delport R, Potgieter HC: Vitamin requirements for the treatment of hyperhomocysteinemia in humans. J Nutr 124: 1927-1933, 1994.
- Clarke R on behave of Homocysteine Lowering Trialists’ Collaboration: Lowering blood homocysteine with folic acid based supplements: meta-analysis of randomised trials. BMJ 316: 894-8, 1998.
- Bostom AG, Shemin D, Lapane KL, Hume AL, Yoburn D, Nadeau MR, Bendich A, Selhub J, Rosenberg IH: High Dose BVitamin treatment of hyperhomocysteinemia in dialysis patients. Kidney Int 49: 147-152, 1996.
- Tremblay R, Bonnardeaux A, Geadah D, Busque L, Lebrun M, Ouimet D, Leblanc M: Hyperhomocysteinemia in hemodialysis patients: effects of 12-month supplementation with hydrosoluble vitamins. Kidney Int 58(2): 851-8, 2000.
- Ducloux D, Aboubakr, Motte G, Toubin G, Fournier V, Chalopin JM, Drüeke T, Massy A: Hyperhomocysteinemia therapy in hemodialysis patients: folinic versus folic acid in combination with vitamin B6 and B12. Nephrol Dial Transplant 17: 865-870, 2002.
- Mamzs B, Hyndman E, Burgess E, Parson H, Schaefer J, Snyder F, Scott-Douglas N: Oral vitamin B12 and high-dose folic acid in hemodialysis patients with hyper-homocysteinemia. Kidney Int 59: 1103-1109, 2001.
- Schnyder G, Roffi M, Pin R, Flammer Y, Lange H, Eberu FR, Meier B, Turi ZG, Hess OH: Decreased rate of coronary restenosis after lowering of plasma homocysteine levels. N Engl J Med 345: 1593-1600, 2001.
- Wrone EM, Homberger JM, Zehnder JL, McCann LM, Coplon NS, Fortmann SP: J Randomized trial of folic acid for prevention of cardiovascular events in end-stage renal disease. J Am Soc Nephrol 15: 420-426, 2004.
- Refsun H, Smith AD, Ueland PM, Nexo E, Clarke R, McPartlin J, Johnston C, Engbaek F, Schneede J, McPartlin C, Scott JM: Facts and recommendations about total homocysteine determinations: an expert opinion. Clin Chem 50: 3-32, 2004.
- Graham IM, Daly LE, Refsum HM, Robinson K, Brattström LE, Ueland PM y cols.: Plasma homocysteine as a risk factor for vascular disease: the European Concerted Action Project. JAMA 277: 1774-1781, 1997.
- Dierkes J, Domrose U, Ambrosch A, Bosselmann HP, Neumann KH, Luley C: Response of hyperhomocysteinemia to folie acid supplementation in patients with end-stage renal disease. Clin Nephrol 51(2): 108-15, 1999.
- Moustapha A, Naso A, Nahlawi M, Gupta A, Arheart KL, Jacobsen DW, Robinson K, Dennis VW: Prospective study of hyperhomocysteinemia as an adverse cardiovascular risk factor in ESRD. Circulation 97: 138-141, 1998.
- Moustapha A, Gupta A, Robinson K, Arheart K, Jacobsen DW, Schreiber MJ, Dennis VW: Prevalence and determinants of hyperhomocysteinemia in hemodialysis and peritoneal dialysis. Kidney Int 55(4): 1470-5, 1999.
- Perna A, Ingrosso D, De Santo N, Galleti P, Brunone M, Zappia V: Metabolic consecuences of folateinduced reduction of hyperhomocysteinemia in uremia. J Am Soc Nephrol 8: 18991905, 1997.
- Ubbink JB,Vermaak WJH, Van de Merwe A, Becker PJ: Vitamin B12, vitamin B6, and folate nutritional status in men with hyperhomocysteinemia. Am J Clin Nutr 57(1): 47-53, 1993.
- Robinson K, Mayer EL, Miller DP, Green R, Van Lente F, Gupta A, Kottke-Marchant K, Savon SR, Selhub J, Nissen SE, Kutner M, Topol EJ, Jacobsen DW: Hyperhomocysteinemia and low pyridoxal phosphate. Circulation 92: 2825-2830, 1995.
- Armada E, Pérez Melón C, Otero A, Gayoso P, Rodríguez M, Esteban J: Efecto de la suplementación con ácido fólico sobre los niveles de homocisteína total en pacientes en hemodiálisis. Nefrología 21: 1671-73, 2001.
- Bostom AG, Shemin D, Gohh RY, Beaulieu J, Bagley P, Massy ZA, Jacques PF Dworkin L, Selhub J: Treatment of hyperhomocysteinemia in hemodialysis patienes and renal transplant recipients. Kid Intern 59 (Supl. 178): 246-252, 2001.
- Sunder-Plassmann G, Fodinger M, Buchmayer H, Papagiannopoulos M, Wojcik J, Kletzmayr J, Enzenberger B, Janata O, Winkelmayer WC, Paul G, Auinger M, Barras U, Horl WH: Effect of high dose folie acid therapy on hyperhomocysteinemia in hemodialysis patients: results of the Vienna multicenter study. J Am Soc Nephrol 11(6): 1106-16, 2000.
- Amadottir M, Brattstrom M, Simonsen O, Thysell H, Hultberg B, Andersson A: The effect of highdose pyridoxine and folie acid supplementation on serum lipid and plasma homocysteine concentration in dialysis patients. Clin Nephrol 40: 236240, 1993.
- Clarke R, Lewington S, Landray M: Homocysteine, renal function and risk of cardiovascular disease. Kid Intern 63 (Supl. 84): 131-133, 2003.
- Nygard O, Nordrehaug J, Refsum H, Ueland P, Farstad M, Farstad M, Vollset S: Plasma homocysteine levels and mortality in patients with coronary artery disease. N Eng J Med 337: 230-6, 1997.
- Wald DS, Law M, Morris JK: Homocysteine and cardiovascular disease: evidence on causality from a meta-analysis. BMJ, vol. 325, 23 nov 2002.
El desarrollo conjunto "Eficacia y seguridad de dos pautasde suplementos vitamínicos sobre los nivelesde homocisteína en pacientes en hemodiálisis. Ensayo clínico prospectivo y randomizado" (J. E. Sánchez Álvarez, L. Pérez Tamajón, D. Hernández, A. Álvarez González, P. Delgado, V. Lorenzo) en forma de un archivo PDF:
El texto original extraído del:
Sánchez Álvarez JE, Pérez Tamajón L, Hernández D, Álvarez González A, Delgado P, Lorenzo V. Eficacia y seguridad de dos pautas de suplementos vitamínicos sobre los niveles de homocisteína en pacientes en hemodiálisis. Ensayo clínico prospectivo y randomizado. Nefrologia 2005;25:288-96.
Documento está distribuida bajo una licencia de:![]() http://creativecommons.org/licenses/by-nc-nd/4.0/
http://creativecommons.org/licenses/by-nc-nd/4.0/
Traducciones
| El artículo "Eficacia y seguridad de dos pautasde suplementos vitamínicos sobre los nivelesde homocisteína en pacientes en hemodiálisis. Ensayo clínico prospectivo y randomizado" en otros idiomas | |
|---|---|
| Efficacy and safety of two vitamin supplement regimens on hyperhomocysteinemia in maintenance hemodialysis (mhd) patients (J. E. Sánchez Álvarez, L. Pérez Tamajón, D. Hernández, A. Álvarez González, P. Delgado, V. Lorenzo) in English: Efficacy and safety of two vitamin supplement regimens on hyperhomocysteinemia in maintenance hemodialysis (mhd) patients |  |


